AJHG | 斑马鱼模型提示GOT2基因相关癫痫性脑病治疗策略

早期婴儿癫痫性脑病会导致运动异常、智力障碍及全面发育落后,预后较差,对患儿的健康造成极大的威胁。在疾病早期进行明确诊断是指导正确治疗的关键。GOT2编码的转氨酶可以催化草酰乙酸和谷氨酸可逆地转化为天冬氨酸和α-酮戊二酸,为线粒体中苹果酸-天冬氨酸穿梭循环(MAS)中的重要部分。近期AJHG杂志发表的文章《Bi-allelic GOT2 Mutations Cause a Treatable Malate-Aspartate Shuttle -Related Encephalopathy》,揭示了GOT2基因在MAS中的重要作用,并进一步建立了GOT2基因突变与癫痫性脑病的关联。研究人员通过建立斑马鱼疾病模型和药效评估,提出吡哆醇及丝氨酸补充可能作为GOT2缺乏患者的治疗策略。该研究为GOT2缺乏患者的生化异常提供了机制解释,并为患者提供了可能的指导治疗方案。

患者临床特征及变异发现
本研究纳入3个无关家庭的4例患儿,4名患儿均存在进行性的小头畸形、进食困难,早期表现为代谢相关的癫痫性脑病,随后出现智力及运动障碍。生化检测结果显示,患者血浆中乳酸含量及血氨含量较高,并且临床症状严重的患者1血浆丝氨酸水平较低。值得注意的是,采用丝氨酸及吡哆醇治疗,显著缓解了其中2例患者的癫痫发作和神经发育缺陷。全外显子检测(WES)结果显示4例患者存在GOT2基因的复合杂合突变及纯合突变,均为框内缺失或错义变异(图1)。Sanger测序证实了GOT2变异的存在及其在家族中的共分离情况。随后研究者进行蛋白建模,预测变异对蛋白功能的影响,结果显示,变异会降低GOT2的催化活性并影响蛋白的整体构象,进而可能影响蛋白的功能。

图1 患者家系和GOT2基因变异信息
GOT2基因变异功能验证
利用患者的成纤维细胞(Fib)进行Western blot,结果显示患者1(P1)GOT2表达显著低于对照组,患者2-4(P2-4)的GOT2表达也有所下降,该结果符合P1展现最严重表型的临床观察。研究者构建了GOT2基因敲除的HEK293细胞系,验证GOT2在Fib及HEK293细胞系中的表达情况与活性水平。Fib实验中,P1-4中GOT2的活性显著低于对照组,分别为对照组平均值的8%,21%,21%和18%,这种缺陷可以被WT GOT2 cDNA挽救。细胞系实验中,GOT2敲除的HEK293细胞系几乎不表达该蛋白,细胞内GOT2蛋白活性也几乎丧失。
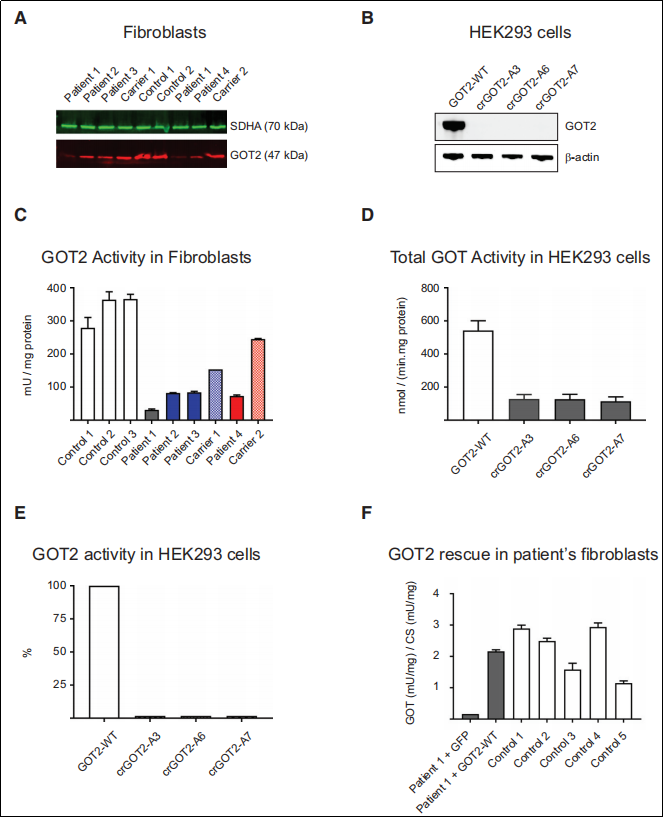
图2 GOT2的表达及活性验证
Fib及HEK293 GOT2-/-中丝氨酸的合成
由于临床发现吡哆醇和丝氨酸治疗对该类癫痫性脑病患者有良好的疗效,故研究者进一步分析了Fib及HEK293 GOT2-/-细胞中丝氨酸的合成情况。结果显示,P1-4患者的Fib中丝氨酸的10小时合成量分别仅有野生型对照的34%,55%,52%和33%,GOT2-/-敲除细胞系中丝氨酸及甘氨酸的合成严重受损。研究者假设这种降低是由于GOT2缺陷影响了MAS过程,导致胞质中NADH/NAD+的比例增加。研究者试图通过恢复细胞氧化还原水平来纠正丝氨酸的合成能力,利用甘油及丙酮酸对细胞系进行孵育,结果显示2.5mmol/L和5mmol/L的丙酮酸可以显著提高丝氨酸与甘氨酸的合成量。
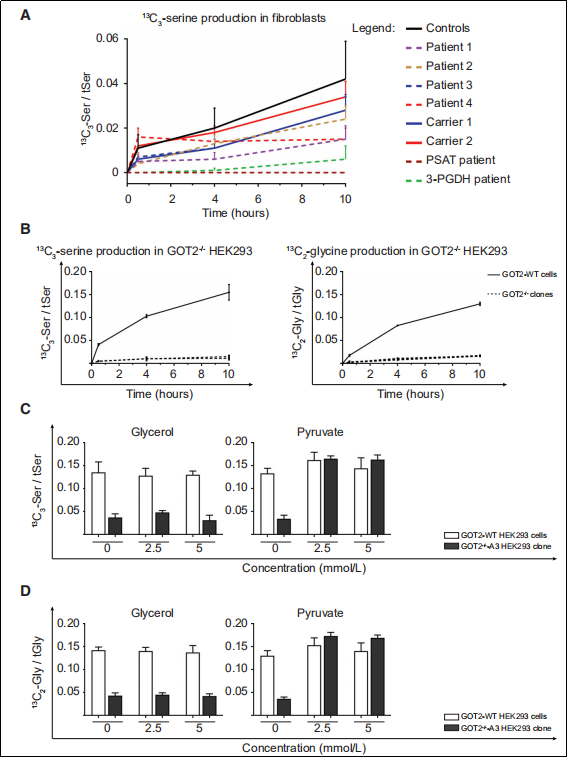
图3 GOT2突变影响丝氨酸的合成
斑马鱼got2a 基因敲降引发癫痫表型
研究者利用Morpholine (MO)技术构建斑马鱼got2a敲降模型,观察到小头畸形、心包水肿、身体弯曲的表型;电生理结果显示,突变斑马鱼出现癫痫样脑电信号,发作次数及持续时间均显著高于野生型。这一结果证实了该基因与癫痫性脑病表型及大脑发育缺陷的关联。研究者随即利用该模型进行治疗干预的探索,采用不同浓度的吡哆醇、丝氨酸、丙酮酸和脯氨酸斑马鱼幼鱼进行干预处理。结果显示吡哆醇和丝氨酸可以挽救got2a 敲降斑马鱼的严重表型,并且提高其生存率,同时减少了癫痫发作的次数及持续时间。该结果为GOT2突变相关癫痫性脑病患者的临床治疗提供了指导依据。

图4 got2a 敲降斑马鱼的表型及药物干预结果
总 结
GOT2缺乏会导致婴儿早期的癫痫性脑病,小头畸形及一系列生化指标的异常。在GOT2缺乏患者中观察到的丝氨酸和甘氨酸合成的减少,可能是由于MAS功能异常导致NADH/NAD+比例升高,进而对NAD依赖的酶和代谢途径产生影响。吡哆醇是丝氨酸生物合成的必要因素,吡哆醇干预可能通过恢复NADH/NAD+的氧化还原平衡,促进丝氨酸的合成。
GOT2缺乏与其他MAS异常的疾病(相关基因:MDH2, SLC25A12, SLC25A13)和丝氨酸代谢疾病(相关基因:PHGDH, PSAT1, PSPH)类似,在临床中需要通过高乳酸、高血氨及低丝氨酸等临床表征对患者进行鉴别诊断。如果这一基因型与表型的关联及治疗策略在更多样本的人群中被证实,GOT2缺乏导致的癫痫性脑病将有望成为可治疗的疾病。
参考文献:van Karnebeek Clara D M,Ramos Rúben J,Wen Xiao-Yan et al. Bi-allelic GOT2 Mutations Cause a Treatable Malate-Aspartate Shuttle-Related Encephalopathy.[J] .Am J Hum Genet, 2019, 105: 534-548.


