来自希望之城国家医疗中心的研究人员开发了一种干细胞模型,用于评估与阿尔茨海默病、帕金森病和肌萎缩侧索硬化症(ALS)等属于同一疾病组的罕见神经系统疾病的治疗方法。这一发现使该研究的资深作者Yanhong Shi博士及其同事离找到减缓或治疗阿尔茨海默病和其它神经退行性疾病的方法更近了一步。
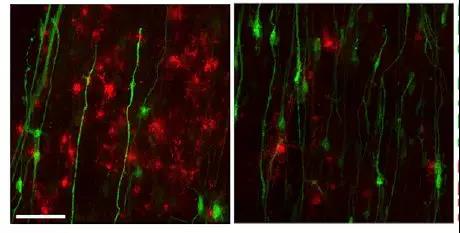
图:亚历山大病患者干细胞衍生的星形胶质细胞(绿色)抑制了前体细胞的生长,该前体细胞随后将分化为髓鞘并加速大脑的沟通交流网络。
该团队从亚历山大病着手研究,因为其病理相对简单。在亚历山大病中,星形胶质细胞中的突变抑制了一种随后将转变为髓鞘的前体细胞,而髓鞘是促进大脑网络内沟通交流的脂肪鞘。
希望之城国家医疗中心的干细胞生物学部主任Shi博士表示,大部分ApoE4存在于星形胶质细胞中,是一种已知会增加阿尔茨海默病风险的基因变异。因此,通过了解星形胶质细胞如何工作,研究人员就可以开发出针对亚历山大病甚至阿尔茨海默病和ALS等其它涉及星形胶质细胞疾病的疗法。
这项研究于8月2日发表在《Cell Stem Cell》杂志上。据报道,该研究首次克服了重大挑战,使科学家们能够了解星形胶质细胞中的GFAP基因突变如何抑制正常髓鞘分布。
在此之前,科学家们无法建立动物模型来观察该病的疾病路径。为此,该研究的主要作者Shi,Li Li和同事们创建了一个干细胞模型,为亚历山大病的疾病通路提供深入见解。他们还开发了一个评估相关神经退行性疾病治疗干预的平台。
研究人员培养了携带GFAP基因突变的源于患者的干细胞,并将其与取自亚历山大病患者的脑细胞进行了平行比较。结果发现两种模型都存在一种称为罗森塔尔纤维的疾病相关蛋白质沉积物。
随后,研究人员使用CRIPSR/Cas9基因编辑技术来纠正病变的星形胶质细胞中的GFAP突变。实验结果表明GFAP突变的纠正减少了与疾病相关蛋白质沉积。接着,研究人员通过使用这种新发现的干细胞疾病模型来检测亚历山大病如何发生及发展。
在亚历山大病中,星形胶质细胞抑制“少突胶质细胞祖细胞”的生长。少突胶质细胞祖细胞是一个能成为髓鞘的前体细胞,其能加速大脑的沟通交流网络。通过比较源于亚历山大病患者和健康对照人群干细胞的星形胶质细胞中不同的基因表达,研究人员发现GFAP突变的星形胶质细胞会分泌CHI3L1蛋白,一种能够抑制神经发育相关过程(包括髓鞘形成)的神经炎症标志物。
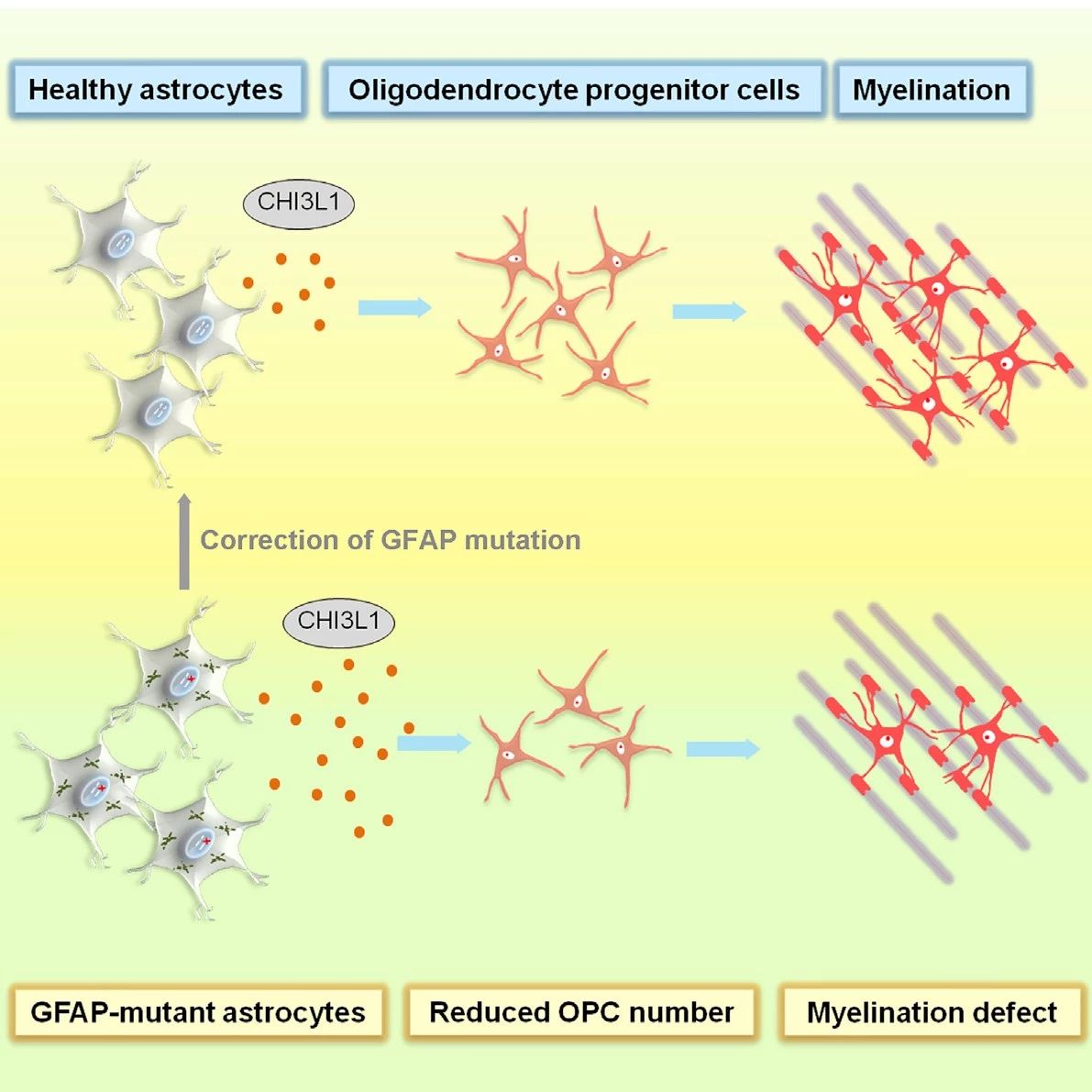
Shi博士表示,靶向CHI3L1的疗法或许可以治疗亚历山大病或减少髓鞘的脑白质营养不良疾病。尽管多年来神经元一直是研究热点,但越来越多的研究发现星形胶质细胞在正常脑功能和神经系统疾病中起着非常重要的作用。星形胶质细胞占大脑细胞的很大一部分,并且在神经炎症中很重要。