GABRA2是小鼠SCN1A和SCN8A癫痫性脑病的遗传修饰因子

基因之间的相互作用在决定遗传性疾病的严重程度中起主要作用。具有相同致病性变异的患者的临床表型受遗传背景差异和正常发育过程中基因表达随机变异的影响。在电压门控钠离子通道基因中已经发现了大量的突变,可以以导致各种形式的癫痫。SCN1A突变可以导致从表型较轻的热性惊厥到表型严重的Dravet综合征等一系列表型;SCN8A突变也可以导致一系列癫痫表型,其中最严重的表型是一种发育性癫痫性脑病,严重受累的患者表现为难治性癫痫发作、发育迟缓、认知障碍、运动障碍和猝死风险增高。但是携带相同钠离子通道变异的患者在临床过程中表型可能有所不同,这表明修饰基因在决定疾病严重程度方面起作用。遗传修饰因子的鉴定有助于了解疾病的发病机制并提出治疗干预措施。小鼠模型为研究癫痫的遗传基础提供了有利工具,小鼠品系背景可以改变表型的严重程度,因此利用近交系小鼠之间的遗传变异来研究并定位钠离子通道基因的遗传修饰因子,可以揭示其基本的生物学机制,并为钠离子通道突变导致的癫痫治疗提供干预的新靶点。本次讨论中涉及的两篇文献,分别报道了GABRA2作为SCN1A和SCN8A所关联的癫痫性脑病的遗传修饰因子的发现过程。

结果SCN1A关联的癫痫表型遗传修饰因子定位
小鼠SCN1A+/-的表型高度依赖于小鼠品系:在129品系中SCN1A+/-小鼠没有明显的表型,小鼠的寿命也是正常的,但是当129.SCN1A+/- 与B6品系杂交得到F1,F1后代中携带SCN1A+/- 的小鼠在8周龄时表现出癫痫发作,并且死亡率达75%。
通过间隔特异性同源性品系定位(interval-specific congenic Strains)将遗传修饰位点精细定位在5号染色体上一段9Mb大小的区域。该区域包含109个已知和预测的基因,其中40个已知在大脑中表达,通过对小鼠129野生型和[129xB6]F1小鼠海马区组织进行转录组测序和差异表达分析筛选出了三个候选修饰基因即Nsun7,Bend4与Gabra2。
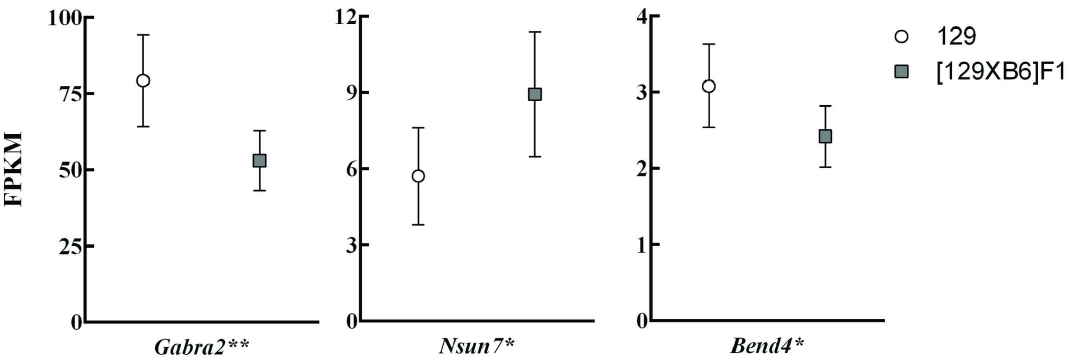
图1:三个候选基因在小鼠海马组织中的表达
对于这三个基因进行功能挖掘发现Nsun7是一种RNA甲基转移酶,其突变会降低人类和小鼠的精子活力;Bend4功能未知,GABRA2编码GABAA受体α2亚基,GABRA2在抑制突触发生中其着关键作用,并且GABA能信号传导功能异常在Dravet综合征中已被报道,因此GABRA2被确定为最佳候选修饰基因。GABRA2在小鼠不同品系前脑组织中展现出差异表达:在129/129纯合品系中表达量最高,129/B6杂合品系中次之,在B6/B6纯合品系中表达量最低,GABRA2蛋白的相对表达与转录水平一致。这意味着高水平的GABRA2表达可能在129.SCN1A+/- 品系小鼠的生存中起到保护作用。
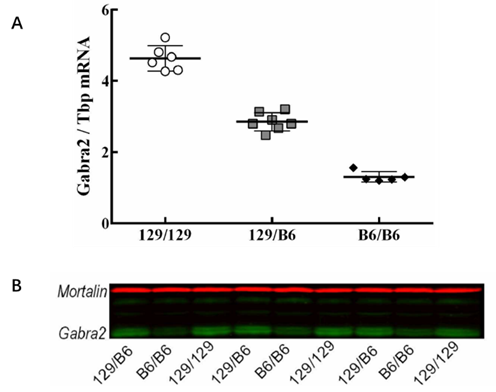
图2 不同品系小鼠前脑组织中GABRA2的转录水平和蛋白表达量
氯巴占是一种对GABRA2亚基具有优先亲和力的抗惊厥药物,通过对F1.SCN1A+/-的饲喂氯巴占进一步评估了GABRA2基因作为候选修饰基因和治疗靶点的作用。小鼠饲喂实验证实氯巴占对热性惊厥有剂量依赖性的保护作用,30 mg/kg剂量的氯巴占对热性惊厥有完全的保护作用,0.3mg/kg和1mg/kg的氯巴占可显著提高小鼠的GTC发作阈值,分别为43.0°C(p<0.0022)和42.9°C(p<0.0079),对照组小鼠热性惊厥发作温度为42.3℃。

图3 氯巴占对热性惊厥剂量保护作用
SCN8A关联的癫痫表型遗传修饰因子定位
小鼠前脑兴奋性神经元中Scn8a-R1872W表达激活的小鼠表现为早期惊厥发作和早亡,利用携带R1872W变异的B6品系小鼠与其它品系小鼠分别进行杂交,结合子代的表型分析和QTL分析,鉴定SCN8A脑病的遗传修饰因子。Scn8aR1872W/+ [B6xSJL]小鼠癫痫发作时间从40日龄至110日龄,寿命从20天至180天以上,中位生存期为66天。Scn8aR1872W/+ [B6xSJL]小鼠与B6小鼠连续回交第三代N3小鼠在20-30日龄开始出现全身性癫痫发作,中位生存期为46天。随着与B6品系回交代数的增加,小鼠癫痫发作时间提早,寿命缩短,截至N8回交世代,突变小鼠的中位生存期降至22天。在回交过程中,SJL品系遗传背景的比例从F2代的50%下降至N8的0.2%,说明来自SJL品系遗传背景中保护性等位基因的缺失可能是导致存活时间缩短的原因。
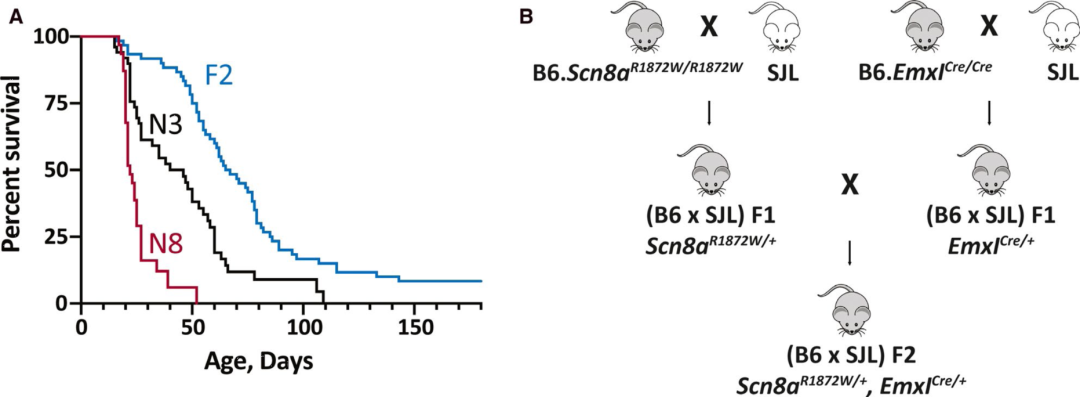
图4 Scn8aR1872W/+,Emx1Cre/+小鼠遗传背景与存活率关系
通过对Scn8aR1872W/+ [B6xSJL]小鼠的数量性状位点(QTL)分析和SNP单倍型检测,该QTL定位在5号染色体67 Mb处的UNC9382069到82 Mb处的S6R053314276之间。在此区间内,Gabra2基因位于71Mb位置。B6小鼠和近缘品系在Gabra2基因5号外显子的剪接受体位点的−3位置携带一个碱基缺失,SJL品系小鼠该位点为野生型,该剪接位点变异的纯合小鼠海马组织中Gabra2转录本的丰度仅为野生型的25%。对Gabra2基因型与癫痫发作表型之间的关系研究发现,Scn8aR1872W/+ [B6xSJL]小鼠中,Gabra2B/B小鼠的中位生存期为53天,明显短于杂合Gabra2B/S和野生型Gabra2S/S小鼠的70天和79天。Gabra2B/B纯合子小鼠的癫痫发作时间中位数为27日龄,早于Gabra2B/S的45日龄和Gabra2S/S小鼠48日龄。这些结果表明, B6品系的小鼠中Gabra2变异导致了小鼠的早期癫痫发作和较短存活时间等更严重表型。
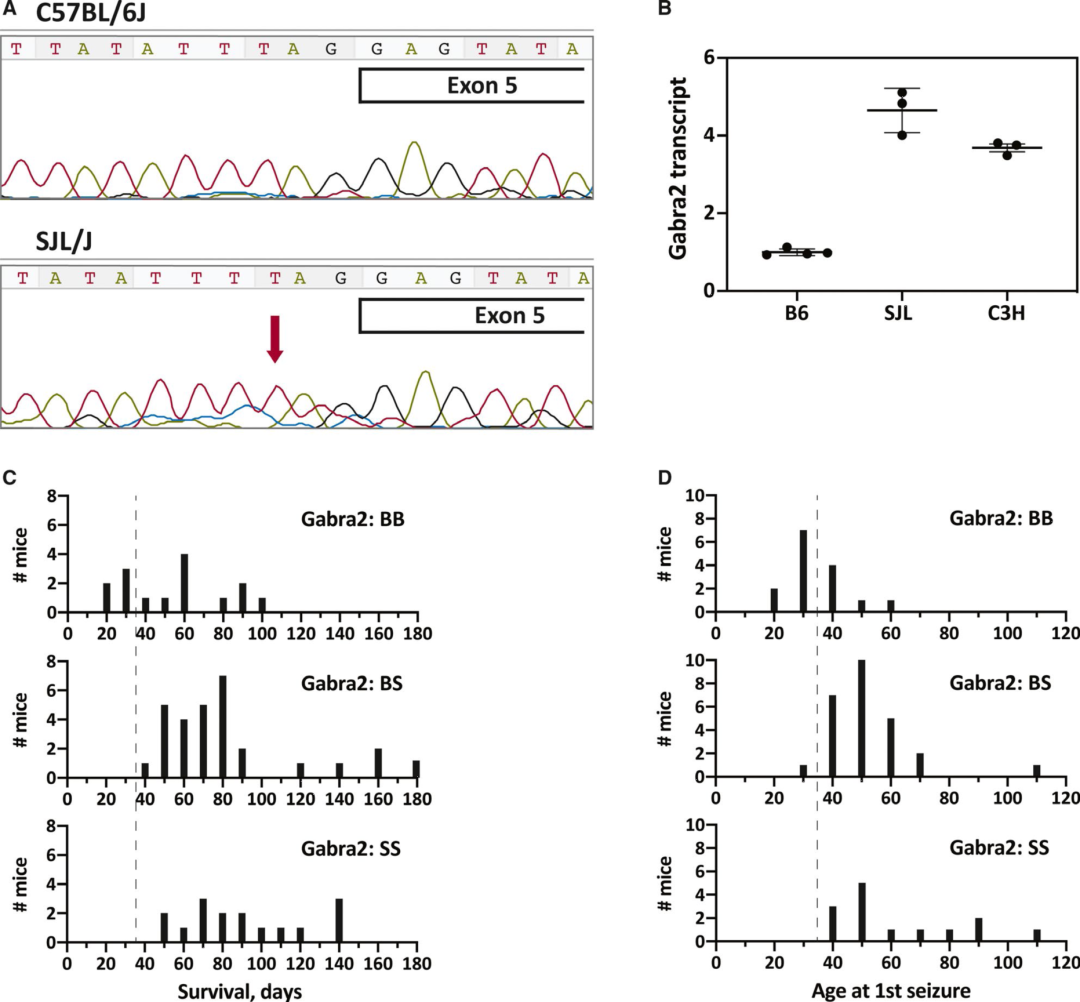
图5 Scn8aR1872W/+,Emx1Cre F2小鼠中Gabra2剪接位点变异与癫痫发作时间和存活时间
讨论
以上研究表明,电压门控钠离子通道基因SCN1A和SCN8A引起的癫痫存在多种修饰因子,可以延缓钠离子通道基因突变引起的癫痫发作并延长携带突变小鼠的寿命,其中一个主要的修饰基因是定位在5号染色体上的Gabra2。Gabra2编码GABAA受体的α2亚基,在海马区高度表达,海马区是癫痫发作产生的重要脑区。SCN1A功能丧失型变异(LOF,loss of function) 或SCN8A功能获得型变异(GOF, gain of function)均可引起两个基因各自所高度表达的抑制型神经元(inhibitory neuron)或兴奋型神经元(excitatory neuron)的异常兴奋而过度放电,进而导致癫痫发作。GABA抑制类神经介质与位于神经元上的GABA受体结合,调节神经元的兴奋性,使其发挥正常功能(图6)。小鼠前脑兴奋性神经元中钠离子通道基因功能获得性突变的表达导致神经元兴奋GABRA2则抑制神经元兴奋度。因此增加的GABA活性可能对具有携带SCN1A LOF与SCN8A GOF变异的患者具有治疗作用。氯巴占是GABA能神经传递的激活剂,对GABRA2亚基具有优先亲和力,也是用作治疗严重癫痫发作的附加药物。因此GABRA2是SCN1A与SCN8A关联的癫痫的潜在治疗靶点。对于GABRA2变异的人群频率研究与导致癫痫发作的单基因变异的相互作用将是未来研究的重要领域。
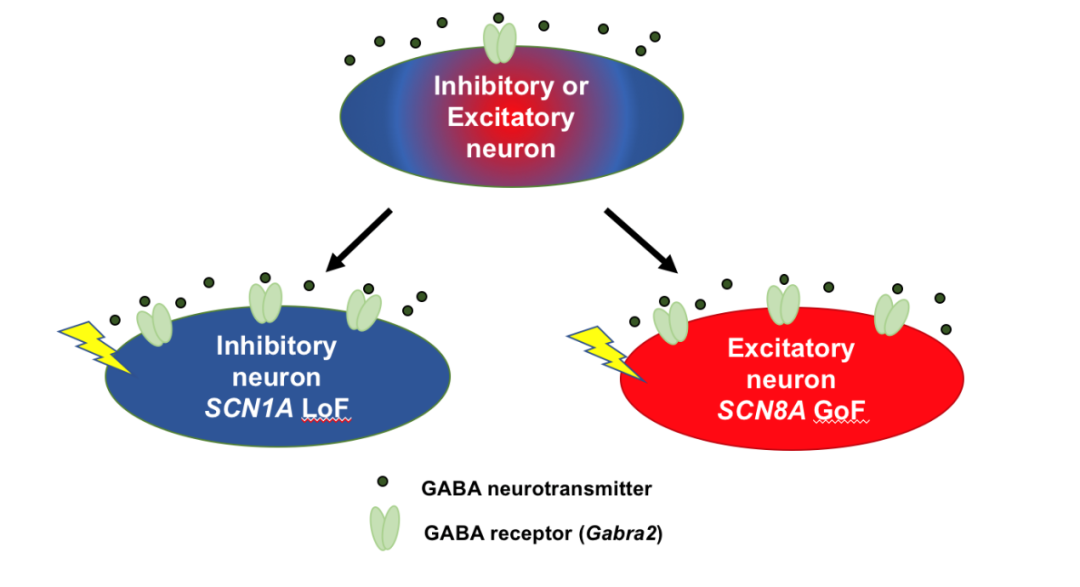
图6 GABRA2/SCN1A及GABRA2SCN8A之间可能的相互作用机制
参考文献:
1. Hawkins NA, Zachwieja NJ, Miller AR, Anderson LL, Kearney JA. Fine mapping of a Dravet syndrome modifier locus on mouse chromosome 5 and candidate gene analysis by RNA‐Seq. PLoS Genet. 2016;12(10):e1006398.
2. Yu W, Hill SF, Xenakis J, Pardo-Manuel de Villena F, Wagnon JL, et al. Gabra2 is a genetic modifier of Scn8a encephalopathy in the mouse. Epilepsia. 2020; 61(12): 2847–2856


